“In een wereld waar de waarheid wordt gemanipuleerd door bewuste keuzes, blijft de detectie van DNA-verontreiniging een onmogelijke opgave. Wat ooit als een onschuldige vergissing werd voorgesteld, onthult nu de schaduwzijde van een systeem dat zijn eigen integriteit heeft opgeofferd. De echo’s van deze keuzes zullen ons blijven achtervolgen, terwijl de gevolgen zich langzaam maar zeker manifesteren in de schaduw van de maatschappij.”
“Dit was geen onschuldige vergissing, maar wijst op bewuste keuzes die effectieve detectie van DNA-verontreiniging onmogelijk maakten.”
Een nieuwe studie in het Journal of Independent Medicine stelt dat bij de productie van mRNA-COVID-19-vaccins van Pfizer/BioNTech en Moderna aanzienlijke hoeveelheden plasmide-DNA in de vaccins zijn achtergebleven. Volgens de auteurs is dit geen toevallig productieprobleem, maar het gevolg van een fundamentele fout in het productie- en testproces, waarbij gebruik is gemaakt van een enzym dat ongeschikt is voor het afbreken van bepaalde DNA-structuren.
De studie, getiteld RNA:DNA Hybrids Survive Digestion in mRNA Vaccine Manufacturing, is geschreven door Kevin McKernan, Charles Rixey en Jessica Rose en werd op 13 januari gepubliceerd. De onderzoekers analyseerden ongeopende vaccinflesjes van Pfizer en Moderna en concluderen dat de hoeveelheid residueel DNA structureel wordt onderschat door de huidige kwaliteitscontroles.
Verkeerd enzym, verkeerd meetresultaat
Bij de productie van mRNA-vaccins wordt plasmide-DNA gebruikt als sjabloon om mRNA aan te maken via een zogeheten in vitro transcriptieproces. Na afloop moet dit DNA worden verwijderd. Volgens de geldende richtlijnen gebeurt dit met het enzym DNase I, dat dubbelstrengs DNA afbreekt.
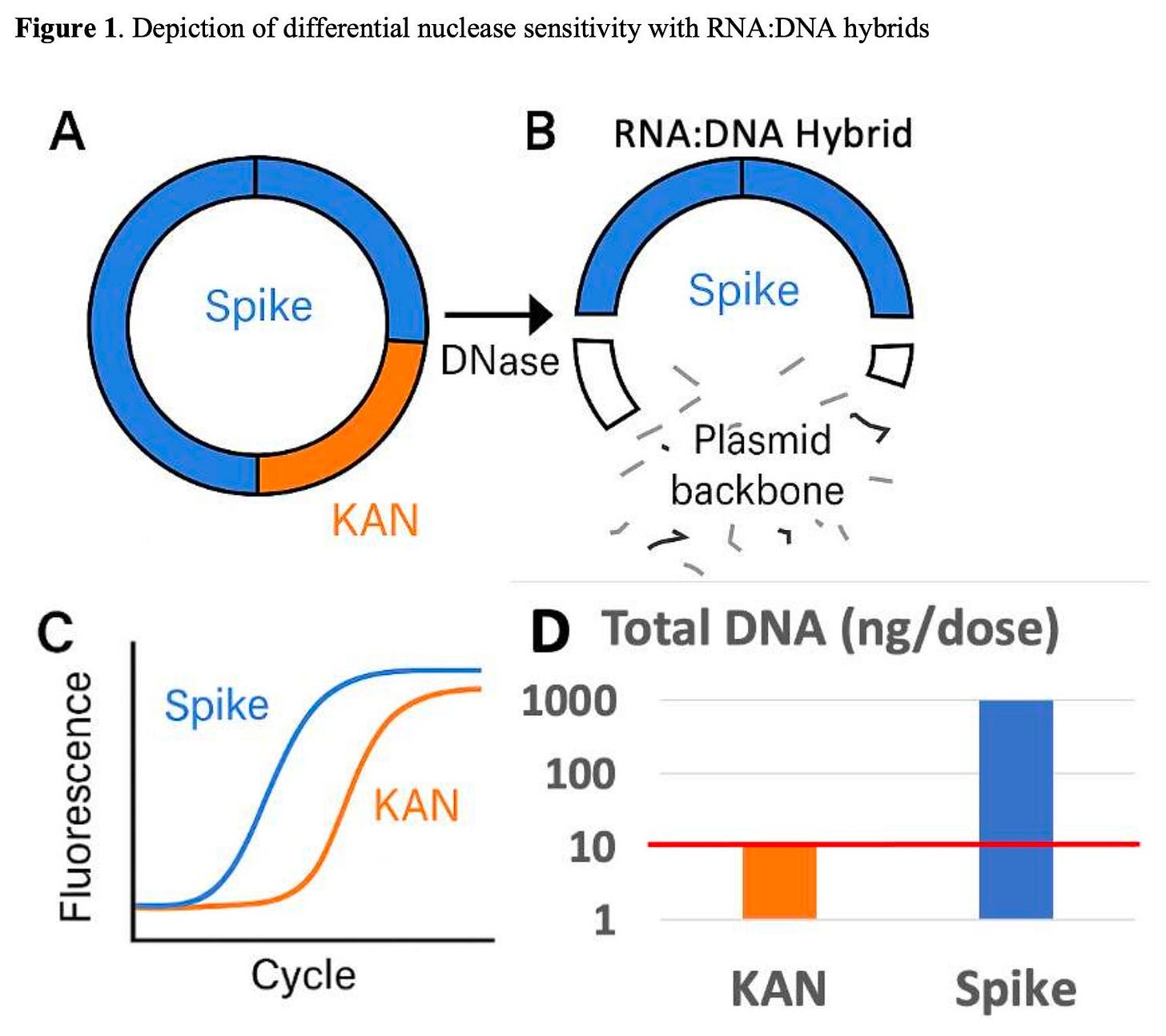
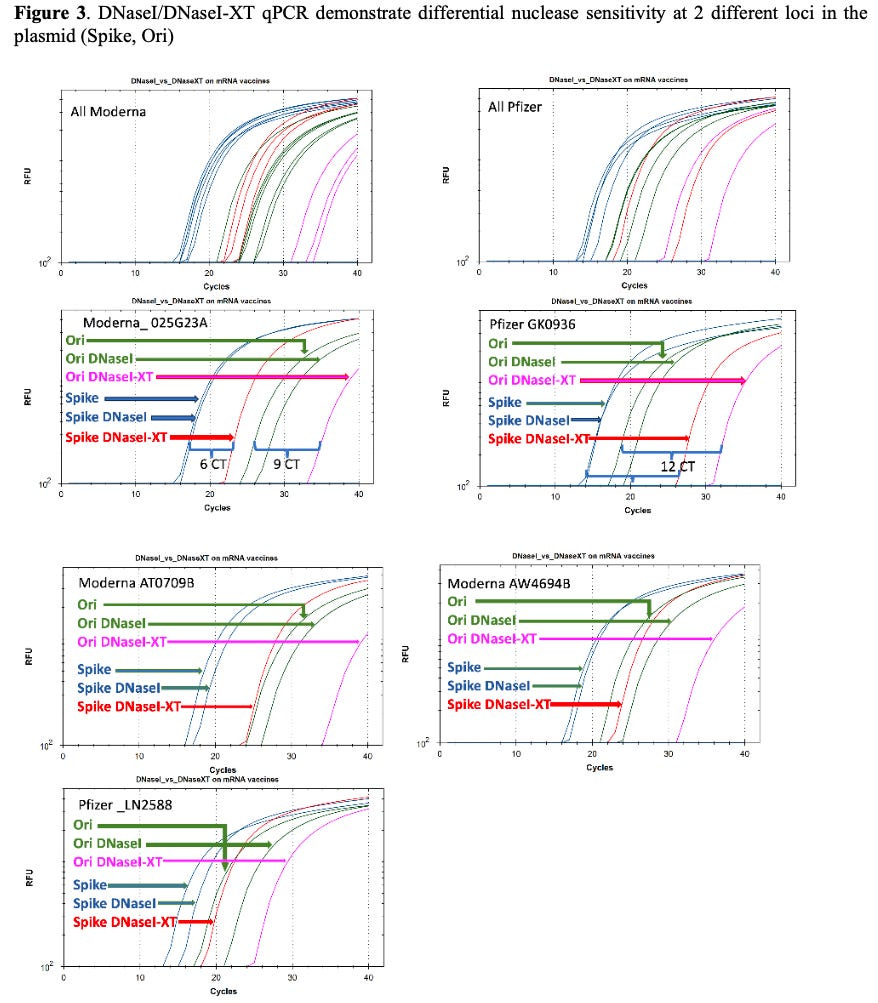
De studie stelt echter dat tijdens dit proces onvermijdelijk RNA:DNA-hybriden ontstaan: structuren waarbij het geproduceerde mRNA zich opnieuw bindt aan het DNA-sjabloon. Deze hybriden blijken grotendeels resistent tegen DNase I. Hierdoor blijft juist het DNA dat het meest actief is geweest in de productie – waaronder delen van het spike-gen – intact.
De auteurs tonen aan dat een alternatief enzym, DNase I-XT, deze hybriden wél effectief afbreekt. Wanneer dit enzym werd gebruikt, nam de afbraak van spike-DNA met een factor 100 tot 1000 toe. Dit laat zien dat DNase I fundamenteel ongeschikt is voor mRNA-vaccinproductie, stellen de auteurs.
Meer DNA dan toegestaan
De onderzoekers gebruikten drie verschillende analysemethoden: qPCR met meerdere primerdoelen, fluorometrie met RNase-behandeling en Oxford Nanopore sequencing. Een hele mond vol. Afhankelijk van de gebruikte methode en het gemeten DNA-gebied liepen de schattingen van residueel DNA meer dan honderdvoud uiteen.
Fluorometrische metingen toonden DNA-hoeveelheden die 15 tot 48 keer hoger lagen dan de door de FDA genoemde bovengrens van 10 nanogram per dosis. Bovendien bleek dat een deel van het DNA opgesloten zat in lipide nanodeeltjes (LNP’s), wat detectie zonder voorbehandeling bemoeilijkt.
Nanopore sequencing bevestigde daarnaast de aanwezigheid van lange DNA-fragmenten, waaronder een fragment van ruim 5000 baseparen dat een groot deel van het spike-gen bevatte. Dit staat haaks op de aanname dat rest-DNA in vaccins slechts uit korte, biologisch irrelevante fragmenten bestaat.
Kritiek op teststrategie van fabrikanten
Een centraal punt van kritiek is dat fabrikanten en toezichthouders grotendeels vertrouwden op één enkele qPCR-test, gericht op het zogeheten KAN-gen (kanamycineresistentie). Dit gen bevindt zich in een plasmidedeel dat geen RNA:DNA-hybriden vormt en wél goed door DNase I wordt afgebroken.
Dit wekt de indruk van lage DNA-verontreiniging, terwijl DNA in andere plasmideregio’s – met name het spike-gedeelte – grotendeels buiten beeld blijft. Opvallend is dat zowel Pfizer als Moderna beschikte over gevalideerde qPCR-assays voor spike-DNA, maar die gebruikten zij niet routinematig voor kwaliteitscontrole.
Mogelijke biologische gevolgen
Hoewel de studie zelf geen klinische effecten onderzoekt, wijzen de auteurs op mogelijke risico’s die nader onderzocht zouden moeten worden. Lang DNA dat verpakt is in LNP’s kan theoretisch cellen binnendringen, mogelijk zelfs de celkern bereiken en daar ongewenste effecten veroorzaken, zoals immuunactivatie of abnormale genexpressie.
RNA:DNA-structuren, ook wel R-loops genoemd, komen van nature in cellen voor, maar zijn in verhoogde hoeveelheden in verband gebracht met DNA-schade, ontsteking en kanker. De auteurs pleiten dan ook voor voorzichtigheid en aanvullend onderzoek.
Scherpe woorden van mede-auteur Rose
Jessica Rose publiceerde naar aanleiding van de studie een uitgebreid Substack-artikel waarin zij verdergaande conclusies trekt. Ze schrijft dat het probleem voorzienbaar en bekend was bij de fabrikanten, mede omdat BioNTech-onderzoekers in eerdere publicaties zelf beschreven dat DNase I nauwelijks werkt op RNA:DNA-hybriden.
Rose stelt dat het gebruik van ongeschikte enzymen en selectieve testmethoden geen onschuldige vergissing was, maar wijst op bewuste keuzes die effectieve detectie van DNA-verontreiniging onmogelijk maakten.
Conclusie
De studie concludeert dat residueel plasmide-DNA in mRNA-vaccins systematisch wordt onderschat door gebrekkige testmethoden en ongeschikte enzymkeuze tijdens productie. De auteurs stellen dat de huidige kwaliteitscontrole tekortschiet en dat strengere controles noodzakelijk zijn.
Gezien de schaal waarop deze vaccins zijn toegediend – vaak verplicht en aan kwetsbare groepen – achten de onderzoekers een grondige herziening van productie- en toezichtnormen dringend noodzakelijk.